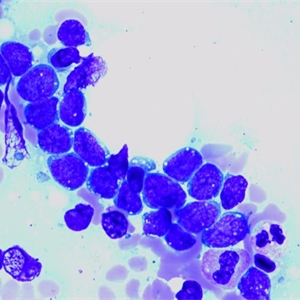
2.在骨髓或外周血涂片中,肿瘤细胞变化较大,可从小的圆形细胞、浆少、核浆比例高、染色质较致密、核仁不清楚的细胞形态(L1)到大的、胞浆相对丰富、核形不规则、染色质分散、多少不等的清晰核仁的细胞形态(L2)。有时可见到胞浆内空泡,这一形态学特点并不是Burkitt淋巴瘤所特有。
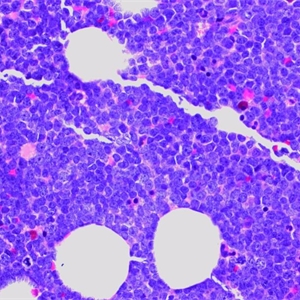
3.骨髓活检常显示细胞密度高,由形态单一的幼稚细胞弥漫浸润代替正常骨髓结构。高倍观察细胞形态同涂片。
4.髓外受累的部位病变通常呈弥漫性分布。有的病例可出现部分淋巴结受累,淋巴母细胞侵犯副皮质区累及生发中心。淋巴母细胞形态一致,圆形至椭圆形核,核膜不同程度卷曲。染色质细点状,核仁通常不明显。大多数病例,核分裂像多,部分病例可见灶性“星空”现象。
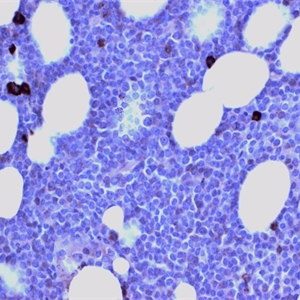
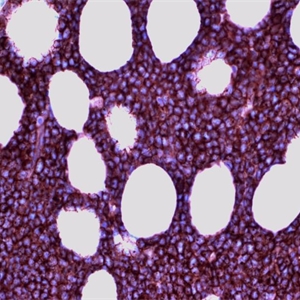
5.免疫表型:几乎所有病例表达CD19、胞浆CD79a和CD22,但其中没任何一个抗原的单一表达具有特异性,要结合其表达特点和其它抗原表达才能确定B系来源;大多数病例CD10、CD22、CD24、PAX5和TdT阳性;CD20、CD34表达不一,CD45可能阴性;CD13、CD33可能阳性。在免疫组化中,CD79a、PAX5常用来确定B系来源,但需注意T-ALL偶也会CD79a阳性。B淋巴母细胞淋巴瘤/白血病可根据细胞的分化程度分为3型:在早期阶段称为早前B(early precursor B-ALL)或原B(Pro-B-ALL),表达CD19,胞浆CD79a、CD22和核TdT;中间阶段称为普通B-ALL(common B-ALL),表达CD10;最成熟阶段称为前B-ALL (Pre-B-ALL),表达胞浆μ,表面免疫球蛋白通常阴性(但阳性也不能排除该型B-ALL的诊断)。
6.遗传学:几乎所有的B-ALL都有Ig重链基因重排。 Ig重链基因重排也可以发生于T-ALL甚至AML,故该检测对细胞系的判定不具特异性。Ig轻链重排也可以发生,且对判定B细胞系来源更有帮助。
根据是否存在重现性遗传学异常及与之相关的临床、表型特征或预后,B-ALL/LBL分为B淋巴母细胞白血病/淋巴瘤-非特指型(B-ALL/LBL,NOS)和B淋巴母细胞白血病/淋巴瘤伴重现性遗传学异常(B-ALL/LBL with recurrent genetic abnormalities) 两大类(见下)。
B淋巴母细胞白血病/淋巴瘤-非特指型(B-ALL/LBL,NOS):符合上述B-ALL/LBL的临床、形态和免疫表型等的一般特征,无特异的重现性细胞遗传学异常,但可以有非特异的异传学改变如缺失6q 、9p 、12p。
B淋巴母细胞白血病/淋巴瘤伴重现性遗传学异常(B-ALL/LBL with recurrent genetic abnormalities):
1)B淋巴母细胞白血病/淋巴瘤伴t(9;22)(q34;q11.2);BCR-ABL 1:为B-ALL中预后最差的亚型。多见于成人,占成人ALL的25%, 但只占儿童ALL的2-4%。肿瘤细胞表达CD10、CD19、TdT,常合表达髓系相关抗原CD13和CD33,但不表达CD117,CD25也常表达(成人)。罕见肿瘤细胞表现为T淋巴母细胞表型。
2)B淋巴母细胞白血病/淋巴瘤伴t(v;11q23);KMT2A重排:KMT2A基因位于11号染色体q23,可与其产生的融合基因有100多个,最常见的是与位于4q21的AF4基因融合,其次是与位于9P13的ENL及9p21.3的AF9融合。该型B-ALL在小于1岁的婴幼儿最多见,较大儿童少见,但至成人发病率又逐渐增加。常表现为白细胞计数显著增高(>100x109),累及中枢神经系统,预后差。肿瘤细胞通常CD19+,CD10-(Pro-B-ALL),并特征性表达NG2类。有时候会同时发现B淋巴母细胞群和单核母细胞群,此时诊断应为B/髓系白血病。
3)B淋巴母细胞白血病/淋巴瘤伴t(12;21)(p13.2;q22.1);ETV6-RUNX1:该融合基因常发生在白血病的早期,但主要见于儿童,而不是婴幼儿;成人罕见。肿瘤细胞常CD19+、CD10+、CD34+,有时CD13+。该型白血病预后很好,儿童治愈率90%以上。
4)B淋巴母细胞白血病/淋巴瘤伴超二倍体:染色体数量增加(>50,<66),结构常为正常。常见于儿童,占儿童B-ALL的25%。 肿瘤细胞表达CD19和CD10,多数CD34+。预后很好,总体治愈率超过90%。
5)B淋巴母细胞白血病/淋巴瘤伴亚二倍体:丢失1条或多条染色体(<46)。根据丢失染色体的多少可分为三种(或四种)亚型:近单倍体(23-29条染色体)、低亚二倍体(33-39条染色体)、高亚二倍体(40-43条染色体)。第四种亚型为近二倍体(44-45条染色体),但定义一般不包括此亚型(预后于前三种不同)。少见,可发生于成人或儿童,单近单倍体亚型仅见于儿童。肿瘤细胞表达CD19和CD10。总体预后较差。低亚二倍体亚型通常同时有TP53突变,近单倍体亚型则常有RAS或受体络氨酸激酶突变。
6)B淋巴母细胞白血病/淋巴瘤伴t(5;14)(q31.1;q32.1);IL3-IGH:5号染色体上的IL3基因与14号染色体上的IGH基因发生重排,导致IL3基因过表达。罕见(<1%),见于成人或儿童。常伴有外周血反应性嗜酸细胞增多。肿瘤细胞表达CD19和CD10。该型预后和其他类型B-ALL无明显不同。
7)B淋巴母细胞白血病/淋巴瘤伴t(1;19)(q23;p13.3);TCF3-PBX1:相对常见于儿童(6%),成人较少见。肿瘤细胞通常表达CD19、CD10和胞浆μ(Pre-B-ALL表型),常CD9强阳性,而CD34阴性或仅少数细胞阳性。早期认为该型预后差,但随着治疗方法的改进,该型预后和其他类型无明显差异,但CNS复发风险可能相对较大。
8)B淋巴母细胞白血病/淋巴瘤,BCR-ABL1样(暂定类型):其基因表达图谱与ALL伴BCR-ABL1相似,但系由于其它酪氨酸激酶基因重排所致;或系由于CRLF2重排(常伴有JAK突变,多见于唐氏综合症);或较少见的情况下累及EPOR基因。此型相对多见(),主要发生于高风险ALL、青少年和成人。预后差,但TKI常有疗效。
9)B淋巴母细胞白血病/淋巴瘤伴iAMP21(临定类型):此型遗传学特点是部分21号染色体段扩增(FISH检测RUNX1基因X5或以上)。见于2%年龄较大儿童,外周白细胞计数常低。预后不好。
2.混合型急性白血病,B/髓系:白血病细胞既表达髓系特异性抗原如MPO又表达B系特异性抗原如cCD22、cCD79a和CD19。
3.Burkitt 淋巴瘤:肿瘤细胞中等大小,但核仁更明显,胞质嗜碱性。表达全B细胞抗原,CD10和Bcl-6也通常阳性,有表面轻链限制性表达。CD34和TdT阴性。
4.AML伴t(8;21):此型AML有时会表达CD19和PAX5,但其典型的细胞形态和表达髓系特异抗原有助鉴别。
5.套细胞淋巴瘤,母细胞样:肿瘤细胞形态与母细胞有相似之处,但表达全B细胞抗原并共表达CD5,cyclin D1阳性。
6.慢性粒细胞白血病(CML)伴淋巴母细胞危象:有CML病史,BCR/ABL+。少数病例首诊时已是淋巴母细胞危象,此时需与原发性B-ALL伴BCR/ABL鉴别。仔细询问回顾病史资料和观察背景细胞形态和密度有助诊断。
7.正常前体B细胞(hematogones)反应性增生:骨髓正常前体B细胞可反应性增生,尤其是儿童,增生可以非常明显,但一般为间质均匀分布,不会弥漫取代造血成分。细胞中等,染色质均匀,无明显核仁。抗原表达类似B淋巴母细胞,但呈现特有的分化成熟谱系如逐渐获得CD20 并丢失CD10、CD34或TdT。