疾病名称:
软组织骨化性纤维黏液样肿瘤
作者:
夏成青 赵明 刘正智
英文名称:
Ossifing Fibromyxoid tumor of soft Tissue,OFMT
在肿瘤中的表达情况:
几乎全部阳性(≥95%的病例阳性):
SNF5通常阳性(<95%,≥75%的病例阳性):
S100经常阳性(<75%,≥55%的病例阳性):
Osteocalcin有时阳性(<55%,≥35%的病例阳性):
CD56少数阳性(<35%,≥15%的病例阳性):
Osteonectin、Desmin、MUC4偶尔阳性(<15%,≥5%的病例阳性):
AE1/AE3、CK-PAN、SMA几乎全部阴性(<5%的病例阳性):
P63、SOX10发病部位:
四肢的近端、头颈部和躯干,少数位于手、足、纵隔或腹膜后
诊断要点:
1.主要发生于中老年,男/女约1.5-2:1,好发于四肢的近端、头颈部和躯干,常表现为缓慢性生长的皮下孤立性结节,少数位于肌肉内;
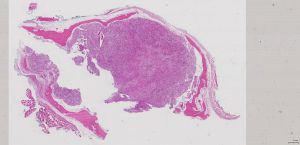
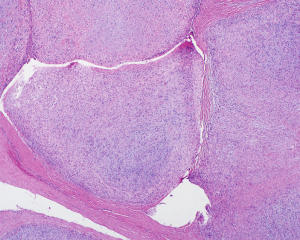
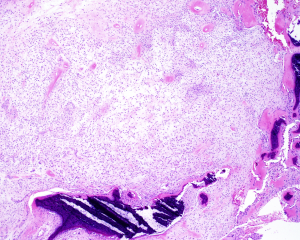
2.肿瘤直径通常<4cm, 大体检查肿瘤呈卵圆形结节状或分叶状,多数有纤维性包膜,典型病例包膜内含有一层薄层的不完整性蛋壳样骨壳, 切面实性伴有粘稠感;恶性转化的肿瘤可突破骨壳向周围组织浸润性生长;
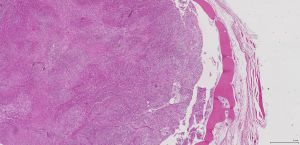
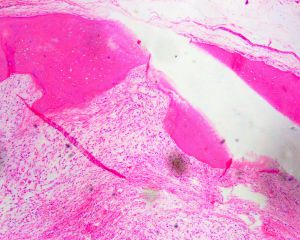
3.镜下80%左右的病例可见骨壳,骨壳由不连续的化生性板层骨组成,小梁周围的骨母细胞缺如或小而不明显,骨小梁可向内深入肿瘤实质内;极个别病例中,骨组织位于肿瘤的中央;
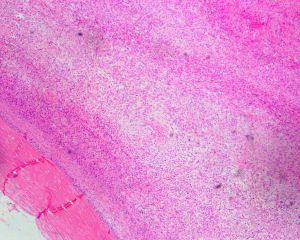
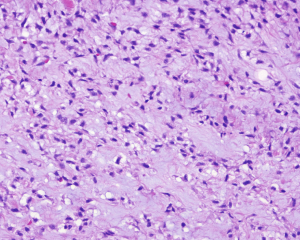
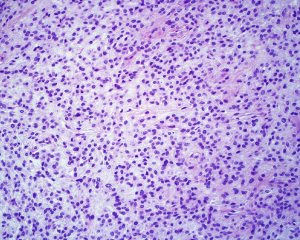
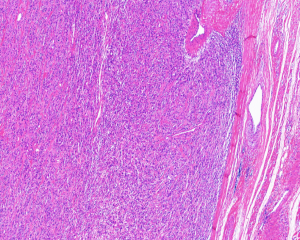
4.肿瘤的实质由多个大小不一、细胞密度不均的小叶组成,小叶内的瘤细胞呈交织索状、梁状、短束状、纤细的网格状排列,有时也可呈马赛克样排列;小叶间为粗细不等的纤维性间隔;
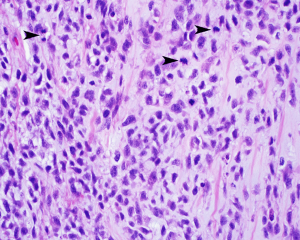
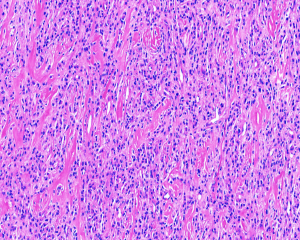
5.细胞圆形、卵圆形或短梭形,大小较一致,胞质淡染或呈嗜伊红色,核染色质细致,核分裂像一般较少见(<2/50HPF),无非典型核分裂象,罕见坏死;
6.瘤细胞间的基质多呈纤维黏液样,或伴多少不等的胶原纤维,部分区域显示明显的玻璃样变性,似骨样基质;
7.部分病例骨壳不明显或仅为局灶性,少数病例包膜内缺乏骨壳结构,可称为“非骨化性纤维黏液样肿瘤”;
8.恶性骨化性纤维黏液样肿瘤的定义标准尚不清楚,瘤细胞密度增高伴弥漫的细胞异型性,核分裂像>2/1 0HPF者,可称为“非典型性或恶性骨化性纤维黏液样肿瘤”。
2.肿瘤直径通常<4cm, 大体检查肿瘤呈卵圆形结节状或分叶状,多数有纤维性包膜,典型病例包膜内含有一层薄层的不完整性蛋壳样骨壳, 切面实性伴有粘稠感;恶性转化的肿瘤可突破骨壳向周围组织浸润性生长;
3.镜下80%左右的病例可见骨壳,骨壳由不连续的化生性板层骨组成,小梁周围的骨母细胞缺如或小而不明显,骨小梁可向内深入肿瘤实质内;极个别病例中,骨组织位于肿瘤的中央;
4.肿瘤的实质由多个大小不一、细胞密度不均的小叶组成,小叶内的瘤细胞呈交织索状、梁状、短束状、纤细的网格状排列,有时也可呈马赛克样排列;小叶间为粗细不等的纤维性间隔;
5.细胞圆形、卵圆形或短梭形,大小较一致,胞质淡染或呈嗜伊红色,核染色质细致,核分裂像一般较少见(<2/50HPF),无非典型核分裂象,罕见坏死;
6.瘤细胞间的基质多呈纤维黏液样,或伴多少不等的胶原纤维,部分区域显示明显的玻璃样变性,似骨样基质;
7.部分病例骨壳不明显或仅为局灶性,少数病例包膜内缺乏骨壳结构,可称为“非骨化性纤维黏液样肿瘤”;
8.恶性骨化性纤维黏液样肿瘤的定义标准尚不清楚,瘤细胞密度增高伴弥漫的细胞异型性,核分裂像>2/1 0HPF者,可称为“非典型性或恶性骨化性纤维黏液样肿瘤”。
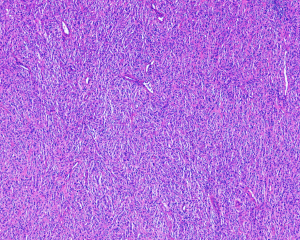
图片:
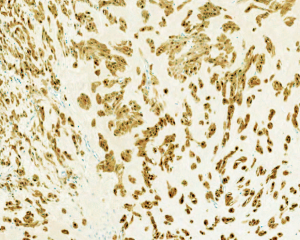
免疫组织化学染色:
肿瘤细胞vimentin、S-100、CD10和NSE阳性,部分病例Leu7、desmin和GFAP阳性,INI-1显示马赛克样的表达缺失,SOX10阴性。
分子标记:
PHF1基因重排
鉴别诊断:
1.神经鞘瘤:无化生性骨壳,可见典型的Antoni A区和Antoni B区交替分布。
2.神经鞘黏液瘤:多位于浅表真皮内,无化生性骨壳。
3.软组织骨肉瘤:肿瘤内能见到肯定的肿瘤性骨样组织,但无骨壳样结构,瘤细胞丰富且异型性明显,核分裂像常见。
2.神经鞘黏液瘤:多位于浅表真皮内,无化生性骨壳。
3.软组织骨肉瘤:肿瘤内能见到肯定的肿瘤性骨样组织,但无骨壳样结构,瘤细胞丰富且异型性明显,核分裂像常见。
预后:
普通的骨化性纤维黏液样肿瘤的生物学进程表现为惰性,完整切除罕见复发和转移;核分裂象>2/10HPF者复发率增高;瘤细胞密度高伴有明显的细胞异型性和核分裂象者,复发和转移率更高。
治疗:
局部扩大切除
参考文献:
Folpe AL, Weiss SW. Ossifying fibromyxoid tumor of soft parts: a clinicopathologic study of 70 cases with emphasis on atypical and malignant variants. Am J Surg Pathol 2003;27:421–31.
Miettinen M, Finnell V, Fetsch JF. Ossifying fibromyxoid tumor of soft parts–a clinicopathologic and immunohistochemical study of 104 cases with long-term follow-up and a critical review of the literature. Am J Surg Pathol 2008;32:996–1005.
Graham RP, Dry S, Li X, et al. Ossifying fibromyxoid tumor of soft parts: a clinicopathologic, proteomic, and genomic study. Am J Surg Pathol 2011;35: 1615–25.