几乎全部阳性(≥95%的病例阳性):
AE1/AE3、EMA、HMGA1、PTEN、CD15、CK7、MSH2、PAX8通常阳性(<95%,≥75%的病例阳性):
HNF-1-beta、p-AKT、Napsin A、Mesothelin、EpCAM、MLH1经常阳性(<75%,≥55%的病例阳性):
met、P21、Annexin-A1、PAX2有时阳性(<55%,≥35%的病例阳性):
CA19-9、mdm2、Hep-Par1、RCC、CA125、PLAP少数阳性(<35%,≥15%的病例阳性):
Alpha-Fetoprotein、CD63、Thrombomodulin、Glypican-3、adipophilin、CEA-M、P27、CyclinD1、S100、Vimentin偶尔阳性(<15%,≥5%的病例阳性):
P16、P53、p-mTOR、TTF-1-cytoplasm、PRP、CD10、SALL4、Calretinin、TTF-1几乎全部阴性(<5%的病例阳性):
SATB2、Beta-catenin、BRAF-V600E、CD146、FOXL2、GATA3、Inhibin、NY-BR-1、SF1、CEA-P、CD163、CDX-2、CK20、PAX5、SOX10、WT-11. 平均发病年龄55岁,常单侧发生;
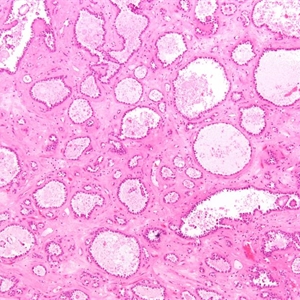
2. 大小不一,平均直径15cm,肿瘤外观与透明细胞腺纤维瘤相似,切面实性、囊实性或以囊性为主;
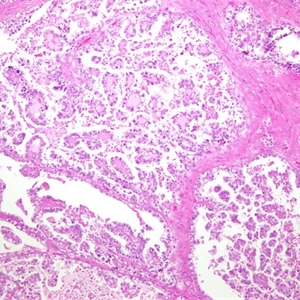
3. 由管囊状、乳头状及实性细胞增生构成,少数病例中可见显著的腺纤维瘤成分;
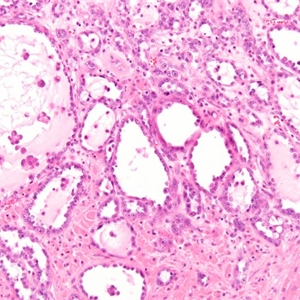
4. 偶尔见显著扩张的囊性结构被覆扁平细胞,给人以良性的错觉;
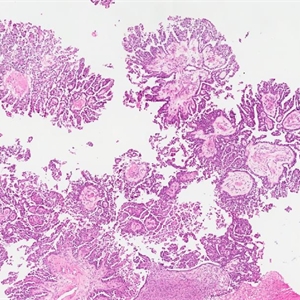
5. 乳头常小而形态规则,也可见大的乳头,间质玻璃样变性,乳头轴心的透明变性是透明细胞癌的典型特征;
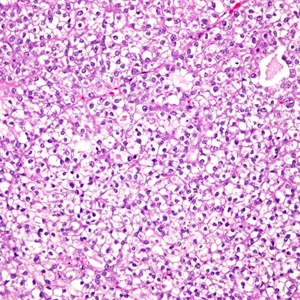
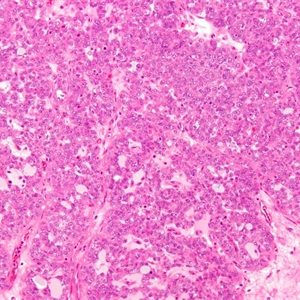
6. 实性区含有丰富透明胞质的多边形细胞呈片状分布,并被纤细的纤维血管间质或致密的纤维间质所分隔;
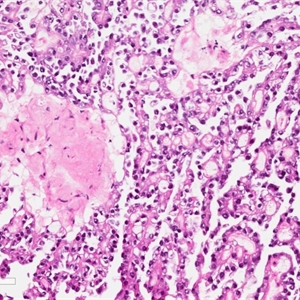
7. 囊管结构为大小不等的管状和囊性结构,细胞核从乳头、腺管或囊腔突起呈靴钉样外观;
8. 细胞胞质透明或含有颗粒状嗜酸性胞质,细胞核多样,从小圆形、多角形到伴有显著核仁的大而多形性核,核分级可以从轻度到显著异型,即使肿瘤中大多数细胞仅表现为轻度核异型,但总能见到显著核异型的细胞;
9. 核分裂活性较低,仅在1/4病例中核分裂像超过10个/10HPF。
10. 可混有浆液性和黏液性肿瘤成分;
11. 肿瘤中可见多少不等的坏死、出血和间质淋巴细胞浸润;
12. 偶见黄素化的间质细胞和砂粒体样钙化;
13. 可伴有子宫内膜异位。
卵黄囊瘤(SYT):
1. 卵黄囊瘤常发生于年轻患者,YST患者血清AFP水平升高,而透明细胞癌发病于中老年,无AFP水平升高;
2. 透明细胞癌的乳头状结构更复杂且含有透明变性的轴心,可与具有乳头样结构的YST相鉴别;
3. YST具有许多透明细胞癌没有的特点,包括特征性Schiller-Duvall小体和网状结构等;
4. 免疫组化染色:透明细胞癌LeuM1阳性和AFP阴性与YST相反;CK7和EMA同时阳性则可排除YST。
1. 无性细胞瘤缺乏透明细胞癌常见的腺囊型和乳头状结构,细胞核更原始;
2. 透明细胞癌缺乏无性细胞瘤常见的间质慢性炎症和肉芽肿;
3. EMA阳性和细胞角蛋白弥漫强阳性有助于排除无性细胞瘤。
浆液性肿瘤:
1. 低-中度细胞核级别的乳头型透明细胞癌可类似浆液性肿瘤: WT1和ER联合应用有助于鉴别诊断,浆液性肿瘤中这两个标记物均为阳性,而透明细胞癌常为阴性;
2. 腺囊型和乳头型结构对透明细胞癌更具特征性,即使肿瘤细胞的胞质不透明,具备上述经典结构也可以诊断为透明细胞癌。与浆液性癌相比,透明细胞癌的乳头结构更纤细、间质透明变性更常见,而浆液性癌中出现局灶肿瘤细胞胞质透明者也并不少见,如果缺乏透明细胞癌中经典的乳头状结构和腺囊状结构时,则不应诊断为透明细胞癌;
3. 高级别浆液性癌WT1、ER通常阳性,HNF-1β阴性,而透明细胞癌中WT1、ER通常阴性,HNF-1β阳性。