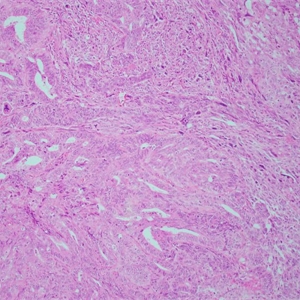
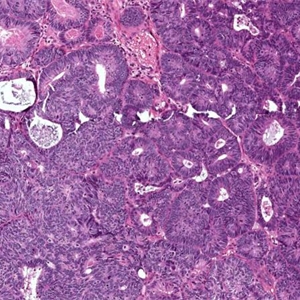
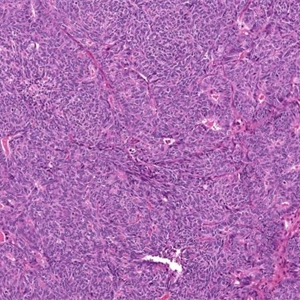
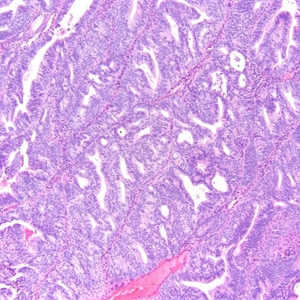
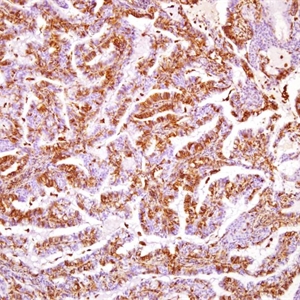
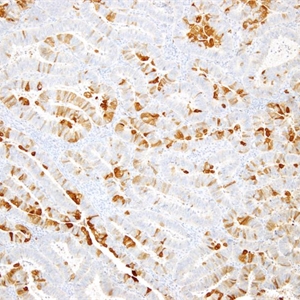
几乎全部阳性(≥95%的病例阳性):
AE1、CA15-3、CAM 5.2、DPC4、SMARCA4、Claudin-5、AE1/AE3、EMA、p16-patchy、CK8、EpCAM通常阳性(<95%,≥75%的病例阳性):
COX-2、pax-8、ER-alpha、PRP、CA125、CK7、NSE、Vimentin经常阳性(<75%,≥55%的病例阳性):
ER、PSMA、CA19-9、p16、Mesothelin、CD117、AR、EGFR、S100有时阳性(<55%,≥35%的病例阳性):
Lysozyme、ER-beta、WT1、Bcl-2、PTEN、p53、DOG1少数阳性(<35%,≥15%的病例阳性):
Beta-catenin-nuc、pax-2、PD-L1、p63、CD7、PLAP、TTF-1偶尔阳性(<15%,≥5%的病例阳性):
MUC5AC、CEA-M、NY-ESO-1、CEA-P、CDX-2、NAPSIN-A、Calretinin几乎全部阴性(<5%的病例阳性):
Glypican-3、SATB2、GATA3、Hep-Par1、pax-5、Brachyury、Chromogranin-A、FLI-1、Inhibin、Uroplakin-3、CK20、GCDFP-15、MUC2、OCT3/4、Podoplanin、PSA、SALL4、SOX10、TFE3、VILLIN1. 子宫内膜腺体密集增生,间质稀少,腺体背靠背;形成筛状,少数病例腺体呈绒毛管状结构;
2. 间质常常胶原化(促结缔组织增生),可伴有泡沫细胞;
3. 周围子宫内膜常呈不典型增生;
4. 细胞不同程度异型;
5. 核分裂多少不等;
6. 可伴有滋养叶细胞分化( hCG+);
7. 根据组织结构和细胞核特征可将子宫内膜样癌分为3级:
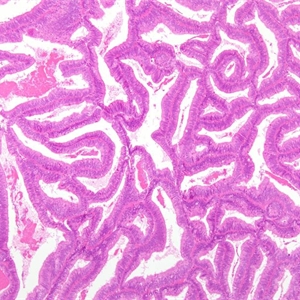
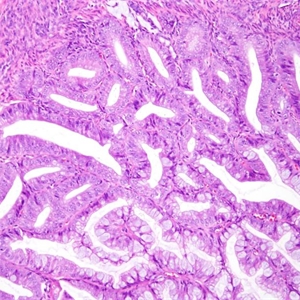
1) 高分化(FIGO I级):
①腺体密集增生,常见出芽、分支,形成乳头状结构,也可呈绒毛管状结构;
②可形成真正的乳头,但细胞无明显异型;
③细胞轻度异型,或灶状中度异型,如异型更严重,FIGO分级升至2级(FIGO 2级)
④常伴良性鳞状分化、灶状黏液分泌或纤毛改变;
⑤除鳞状分化或桑椹样区域外,实性区域≤5%。
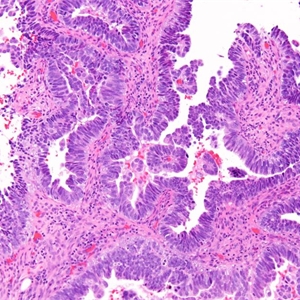
2) 中分化(FIGO 2级):
①除鳞状分化或桑椹样区域外6%-50%区域为实性无腺样结构区;
②肿瘤细胞中度异型,核仁明显,如出现3级核(细胞核显著增大、多形性,染色质粗糙、分布不均匀,并有明显的嗜酸性核仁),FIGO分级升为 3级。
3)低分化(FIGO 3级)
①除鳞状分化或桑椹样区域外>50%区域为实性无腺样结构区;
②肿瘤细胞具有高级别核;
③腺体分化差,可存在鳞状细胞癌成分;
④淋巴管血管浸润常见。
8.2020年第五版WHO肿瘤分类将宫体子宫内膜样癌分为4型:
8.1 POLE-超突变型:POLE突变;多表现为形态学高级别,形态学特征不明显伴有散在肿瘤性大细胞,肿瘤淋巴细胞浸润明显,预后最好。
8.2 MMR-deficienct:免疫组化染色MHL1、MSH2、MSH6、PMS21个或多个缺失,分子检查示MSI 。
8.3 p53突变型:免疫组化染色p53,弥漫(>60%的细胞)强阳性或完全阴性;
8.4 无特异性分子特征型:缺乏上述分子改变。
低级别宫内膜样腺癌ER、PR弥漫强阳性,p16可斑片状阳性。
2-5%的低级别宫内膜样癌和20%的高级别宫内膜样癌p53表达异型(弥漫强阳性或完全阴性)
广谱CK,EMA,CA125,vimentin等常阳性,CEA的表达不定;几乎所有的子宫内膜样癌都表达CK7而不表达CK20;少数有黏液样分化的亚型也表达CDX2。
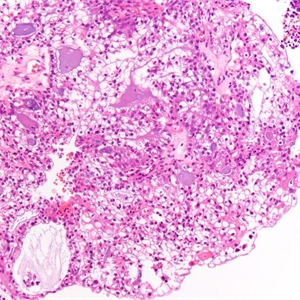
Arias—Stella反应
1. 对育龄女性来说,Arias-Stella反应远比子宫内膜癌常见,尤其是当临床病史提示存在近期妊娠时,但年轻女性甚至妊娠时也可发生内膜癌;
2. 与子宫内膜癌不同,Arias-Stella反应更多地呈多灶性,并且混合有分泌腺体和蜕膜组织;
3. Arias-Stella反应内的腺体可以复杂弯曲,但缺乏融合或乳头状生长模式,间质也无促结缔组织增生反应;
4. Arias-Stella反应腺上皮的核可以显著增大,但核染色质退变、污浊,核分裂像非常少见。
月经期子宫内膜:间质崩解导致了不同大小腺体片段和间质细胞簇与血液的杂乱混合,看起来很像恶性。
1. 腺上皮是温和的,并且表现有分泌活动;
2. 可以识别出邻近未受损的子宫内膜片段中混有前蜕膜细胞,这对鉴别诊断有帮助。
子宫颈腺癌:免疫标记对鉴别二者有帮助
1. 典型子宫内膜癌的表达模式是p16灶(+)/ER(+)/PR(+),而典型子宫颈腺癌则为p16弥漫(+)/ER.(-)/PR(-);
2. 宫颈癌常CEA阳性,Vimentin阴性,而子宫内膜样癌常CEA阴性,Vimentin阳性。
浆液性癌:高级别宫内膜样癌与浆液性癌有时鉴别困难,高级别宫内膜样癌常呈实性,细胞多形性不显著。当细胞异型性明显超出组织结构异型性时应想到浆液性癌的可能;免疫组化染色ARID1A、PTEN或一种错配修复蛋白丢失时支持高级别宫内膜样癌;p53异常表达更支持浆液性癌。