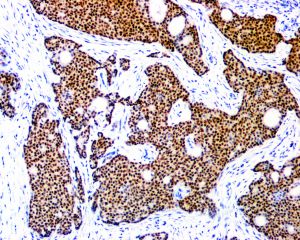
几乎全部阳性(≥95%的病例阳性):
AE1、CA15-3、CAM 5.2、CK-PAN、HMFG、Lewis-Y、P21、PKK1、AE1/AE3、CK18、CK8、MUC4通常阳性(<95%,≥75%的病例阳性):
BCA-225、Beta-Catenin-mem、CD95-fas、EMA、ER、GATA3、MUC3、TIMP-1、TIMP-2、CD24、CD64、COX-2、VEGF、CK19、CK7、E-cadherin、EpCAM经常阳性(<75%,≥55%的病例阳性):
GLUT1、CA9、CAIX、FLI-1、NY-BR-1、PRP、CD138、CD15有时阳性(<55%,≥35%的病例阳性):
AE3、androgen receptor、BCL-2、CEA-M、Thrombomodulin、adipophilin、Beta-catenin、CD44、CD75、MUC5AC、Clusterin、P504s、CyclinD1、GCDFP-15、Mammaglobin少数阳性(<35%,≥15%的病例阳性):
CD146、CD45RO、P27、FVIII、FVIIIRAg、HBME-1、HER2、P53、RCC、TAG72、Claudin-1、CEA-P、CD117、CD5、PLAP、Podoplanin、S100、Synaptophysin偶尔阳性(<15%,≥5%的病例阳性):
Beta-catenin-nuclear、CA19-9、HCG-alpha、lysozyme、mdm2、Mesothelin、TGF-beta-1、CA125、CD10、CD7、CK14、CK5/6、MUC2、NSE、SOX10、Calretinin几乎全部阴性(<5%的病例阳性):
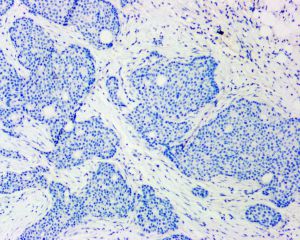
34bE12、Alpha-Fetoprotein、Cathepsin-K、CD20、CD271、CD63、CD74、CK1、Hep-Par1、melan-A、OCT4、P40、P63、PAP、PGP9.5、PNL2、PSMA、vegfr2、TLE1、Arginase-1、Calponin、CD163、CD2、CD3、CD30、CD31、CD34、CD4、CD56、CD57、CD68、CD8、CDX-2、CgA、CK20、CK5、NAPSIN-A、PAX5、PAX8、PSA、SALL4、VILLIN、Vimentin、WT-1、SMA1. 组织学形态不一,缺乏规律性的结构特征。
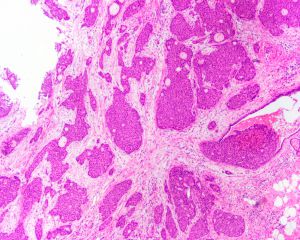
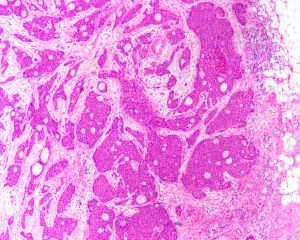
2. 肿瘤细胞可排列成条索状、簇状、小梁状、巢状或片状实性。部分病例腺样分化明显,或在肿瘤细胞巢团中形成具有腔隙的管状结构。偶尔可见一些具有单层线状浸润或靶环状结构的区域,类似于浸润性小叶癌。
3. 肿瘤细胞一般体积较大,形态各异,异型性明显,细胞间界限清楚或融合呈合体细胞样。胞质较丰富,略呈嗜酸性。核大小一致或高度异型,可有多个明显的核仁,核分裂像多少不等。
4. 可有鳞状化生、大汗腺化生或透明细胞变。
5. 相当部分病例可见导管原位癌病灶,少数可见小叶原位癌。
6. 间质成分多少不一,可以为致密的胶原化间质,也可为富于细胞的纤维性间质。
7. 常见钙化现象,钙化可在肿瘤坏死区出现,也可在导管原位癌中出现。
8. 部分病例可见显著的淋巴细胞、浆细胞浸润,甚至出现肉芽肿样反应。
9. 癌组织常侵犯血管、淋巴管,也常见神经周围浸润。
10. 肿瘤边缘呈浸润性生长,也可呈膨胀性生长。
11.除上述组织学特征外还包括下列特征性形态学图像(pattern)
富于糖原(透明细胞)
皮脂腺癌
上述特征的癌在2012年版本均作为独立的形态学亚型。
1. 硬化性腺病常保留小叶轮廓;
2. 硬化性腺病常可见上皮细胞和肌上皮细胞两种细胞;
3. 硬化性腺病细胞巢或条索周围可见完整的基底膜,IV型胶原及层黏蛋白染色可清楚显示;
4. 肌上皮细胞标记(p63、34βE12、SMA等)可显示肌上皮细胞存在。
1. 放射状瘢痕/复杂硬化性病变具有其形态学特征:中心为胶原性瘢痕,纤维化及弹力纤维增生,小导管增生,放射状排列;
2. 放射状瘢痕/复杂硬化性病变增生变形的腺管及病变细胞形态温和,无细胞异型性,坏死少见;
3. 假浸润病变仅局限于瘢痕区,不浸润至周围脂肪组织。而真性浸润的癌成分,细胞多有明显异型性,并不只局限于瘢痕区,常会有周围乳腺组织或纤维脂肪组织的浸润,并伴有反应性纤维增生性间质,腺管周围没有肌上皮。
4. 放射状瘢痕/复杂硬化性病变细胞巢/条索周围有肌上皮细胞围绕,免疫组化肌上皮标记阳性。值得注意的是,少数放射状瘢痕/复杂硬化性病变病例中央假浸润腺管肌上皮可缺失,需要全面观察作出判断。
微腺性腺病含有嗜伊红分泌物的小的圆形小管在乳腺组织中散在分布的一种罕见病变,没有肌上皮存在,也不表达ER、PR和Her-2,但是S-100强阳性。如果发现分化好的乳腺癌但是ER、PR阴性时应该除外该病变,微腺性腺病可以局部复发,但不转移。
特殊类型乳腺癌
约25%的乳腺浸润性癌归类为特殊类型的乳腺癌,其中预后好的有小管癌、筛状癌、粘液癌、乳头状癌、Ⅰ-Ⅱ级的小叶癌、腺样囊性癌,预后不良的有化生性癌和微乳头状癌;大多数特殊型乳腺癌要求有至少90%的可识别的特殊类型乳腺癌成分,如果特殊类型乳腺癌成分为10-90%之间则归类为混合型非特殊型浸润性癌-特殊类型癌。
部分非特殊型浸润癌可有癌细胞单排队列状分布的情况,甚至可见癌细胞条索环绕正常导管类似靶环状的区域,需要与小叶癌鉴别。
1. 多数小叶癌基本不形成实性、腺泡状、乳头状、腺样结构,而呈单排或双排条索状分布;
2. 小叶癌癌细胞相对较小,细胞间连接松散,与导管癌细胞间黏附紧密不同;
3. 免疫组织化学染色浸润性小叶癌E-cadherin阴性或弱阳性,p120呈胞质阳性,而导管癌E-cadherin一般强阳性,p120为胞膜阳性。
1. 小管癌是一种高分化的浸润性癌,细胞规则排列成明确的小管;
2. 小管癌的导管结构形态多不规则,可形成角,管腔相对一致,圆形或卵圆形,衬覆细胞为单层。导管癌的管状结构多在癌细胞条索或小巢中出现,管腔的形状、大小不一,衬覆细胞常为多层;
3. 小管癌细胞一般较小,异型不明显,而浸润性导管癌细胞体积相对较大,胞质丰富,细胞有不同程度的异型性。